در این نوشته با جواب با هم بیندیشیم صفحه 39 شیمی دهم همراه شما هستیم.
جواب با هم بیندیشیم صفحه 39 شیمی دهم
هر ترکیب یونی از لحاظ بار الکتریکی خنثی است؛ زیرا مجموع بار الکتریکی کاتیونها با مجموع بار الکتریکی آنیونها برابر است. از این ویژگی میتوان برای نوشتن فرمول شیمیایی ترکیبهای یونی دوتایی بهره برد؛ برای نمونه به چگونگی تشکیل سدیم سولفید و آلومینیم اکسید و نوشتن فرمول شیمیایی آنها توجه کنید.
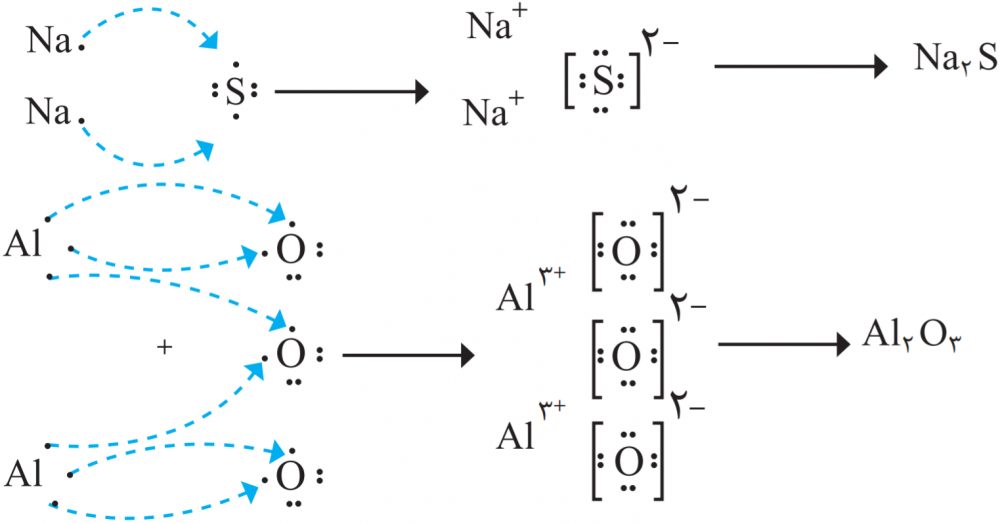
١- روشی برای نوشتن فرمول شیمیایی ترکیبهای یونی دوتایی ارائه کنید.
فلزها به تعداد الکترونهای ظرفیت خود، به نافلزها الکترون میدهند و در نتیجه فلزها به کاتیون و نافلزها به آنیون تبدیل میشوند.
در فرمول شیمیایی تعداد کاتیون و آنیونهای به دست آمده را در اندیس (زیر) هر کدام قرار میدهیم. در فرمول شیمیایی فلز در سمت راست و نافلز در سمت چپ قرار میگیرد.

2- فرمول شیمیایی هر یک از ترکیبهای زیر را بنویسید.
آ) کلسیم برمید CaBr2
ب) پتاسیم نیترید K3N
پ) منیزیم سولفید MgS
ت) آلومینیم فلوئورید AlF3
3- با توجه به دادههای جدول زیر، شیوۀ نام گذاری ترکیبهای یونی دوتایی را مشخص و جدول صفحۀ بعد را کامل کنید.
ابتدا نام کاتیون را در سمت راست نوشته و سپس نام آنیون را در کنار آن وارد میکنیم.
| نام و نماد شیمیایی کاتیون | نام و نماد شیمیایی آنیون | ||
|---|---|---|---|
| یون لیتیم | Li+ | یون برمید | Br− |
| یون پتاسیم | K+ | یون یدید | I− |
| یون منیزم | Mg2+ | یون نیترید | 3N− |
| یون کلسیم | Ca2+ | یون سولفید | S2− |
| یون آلومینیم | Al3+ | یون فلوئورید | F− |
| فرمول شیمیایی | نماد یونهای سازنده | نام ترکیب یونی |
|---|---|---|
| MgO | Mg2+ ، O2− | منیزیم اکسید |
| CaCl2 | Ca2+ ، Cl1− | کلسیم کلرید |
| K2O | O2− ، K+ | پتاسیم اکسید |
| Na3P | p3− ، Na+ | سدیم فسفید |
| LiBr | Br− ، Li+ | لیتیم برمید |
سایر صفحات گام به گام شیمی دهم
- جواب با هم بیندیشیم صفحه ۳۷ شیمی دهم
- جواب با هم بیندیشیم صفحه ۳۹ شیمی دهم
- جواب خود را بیازمایید صفحه ۴۱ شیمی دهم
- جواب تمرین های دوره ای فصل ۱ شیمی دهم