جواب تمرین های دوره ای فصل ۱ شیمی دهم ✅ صفحه ۴۲ تا ۴۶

در این نوشته با جواب تمرین های دوره ای فصل ۱ شیمی دهم رشته تجربی و ریاضی همراه شما هستیم.
جواب صفحه ۴۲ شیمی دهم
۱- بررسی نمونهای از یک شهاب سنگ نشان داد که در این شهاب سنگ ایزوتوپهای۵۷Fe ۵۶Fe ،۵۴Fe وجود دارد.
آ) آرایش الکترونی ۲۶Fe را رسم کنید.

ب) موقعیت آهن را در جدول دوره ی عنصرها مشخص کنید.
دوره ۴، گروه ۸
پ) آهن به کدام دسته از عنصرهای جدول تعلق دارد؟
آهن به دسته d تعلق دارد، چون زیر لایه d این عنصر در حال پر شدن میباشد.
ت) آیا آرایش الکترونی ایزوتوپهای آهن یکسان؟ چرا؟
بله، چون ایزوتوپها عدد اتمی یکسانی دارند و در یک اتم خنثی تعداد الکترون و پروتون برابر است. دقت کنید که در نوشتن آرایش الکترونی، تعداد الکترونها را در نظر میگیریم. چون ایزوتوپها الکترونهای برابری دارند، پس آرایش الکترونی آنها مشابه است.
۲- با استفاده از آرایش الکترون نقطهای اتمها در هر مورد، روند تشکیل، نام و فرمول شیمیایی ترکیب یونی حاصل از واکنش اتمهای داده شده را مشخص کنید.

۳- با توجه به شکل
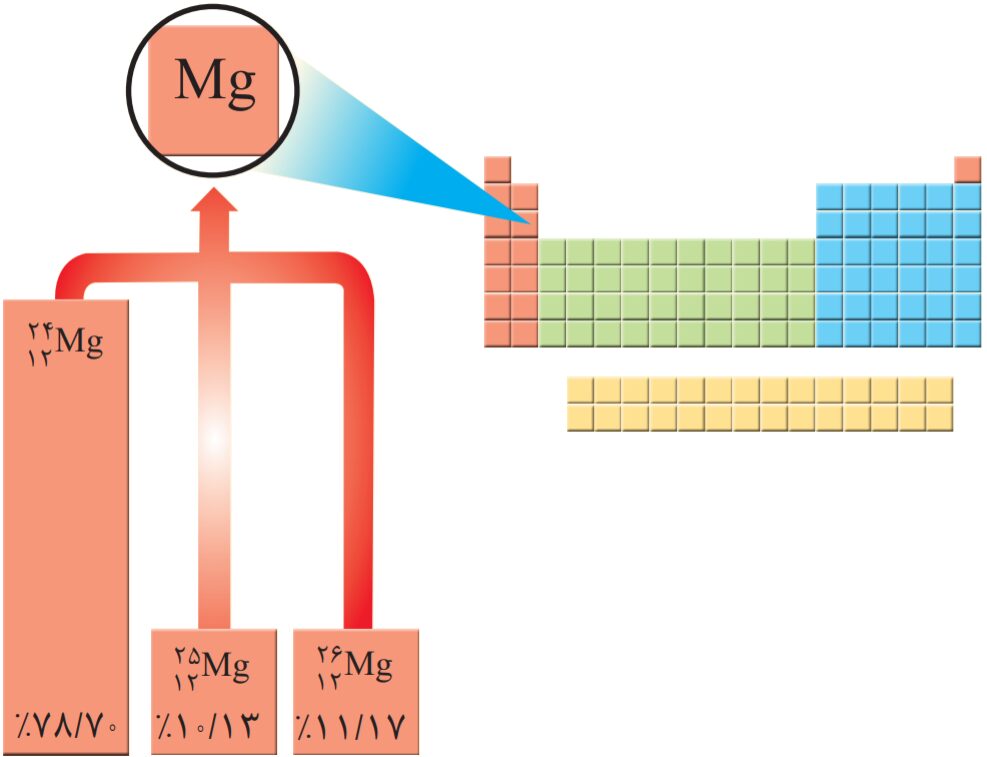
آ) جرم اتمی میانگین منیزیم را به دست آورید.

ب) مفهوم هم مکانی را توضیح دهید.
ایزوتوپ به معنی هم مکان می باشد و اتمهایی که ایزوتوپ یکدیگرند در جدول تناوبی در یک خانه قرار میگیرند.
۴- هرگاه یک جریان الکتریکی متناوب و ۱۱۰ ولتی به یک خیار شور اعمال شود، خیارشور مانند شکل زیر شروع به درخشیدن میکند. علت ایجاد نور رنگی را توضیح دهید.
در خیار شور یونهای مثبت (سدیم) و منفی (کلر) وجود دارد. هرگاه جریان برق با ولتاژ بالا (۱۱۰ ولت) را از درون خیار شور عبور دهیم. یونهای سدیم با جذب انرژی جریان برق، از خود پرتوهای الکترومغناطیس گسیل میدارد که برای فلز سدیم نگ آن زرد است.
جواب صفحه ۴۳ شیمی دهم
۵- آرایش الکترونی اتمهای باریم و ید به شما داده شده است؛ با توجه به آن:
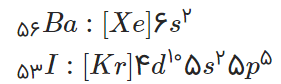
آ) پیش بینی کنید که هر یک از اتمهای باریم و ید در شرایط مناسب به چه یونی تبدیل میشود؟
اتم باریم فلزی بوده و با از دست دادن الکترونهای ظرفیتی خود به آرایش گاز نجیب Xe تبدیل میشوند و یون +Ba2 ایجاد میکنند اتم یُد نافلزی بوده و با گرفتن یک الکترون به آرایش گاز نجیب Xe تبدیل شده و یون -I ایجاد میکند.
ب) فرمول شیمیایی ترکیب یونی حاصل از واکنش باریم با یُد را بنویسید.
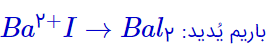
۶) اگر میانگین جرم هر اتم بور در حدود ۲۳-۱۰×۱.۷۹۳ گرم باشد، جرم مولی آن را حساب و با جدول دوره ای مقایسه کنید.

۷- گرافیت دگر شکلی از کربن است. در قرن شانزدهم میلادی قطعۀ بزرگی از گرافیت خالص کشف شد که بسیار نرم بود. به دلیل شکل ظاهری گرافیت، مردم در آن زمان میپنداشتند که گرافیت از سرب تشکیل شده است. امروزه با آنکه میدانیم مغز مداد از جنس گرافیت است، اما این ماده همچنان به سرب مداد معروف است. در ۰/۳۶ گرم گرافیت خالص، چند مول کربن و چند اتم کربن وجوددارد؟

۸- در جدول روبه رو عنصرهایی نشان داده شده است که در دما و فشار اتاق به شکل مولکولهای دو اتمی وجود دارند. با استفاده از آرایش الکترون نقطهای، ساختار این مولکولها را رسم کنید.

۹- هر یک از شکلهای زیر برشی از اتم یک عنصر را نشان میدهد؛ با توجه به آن:
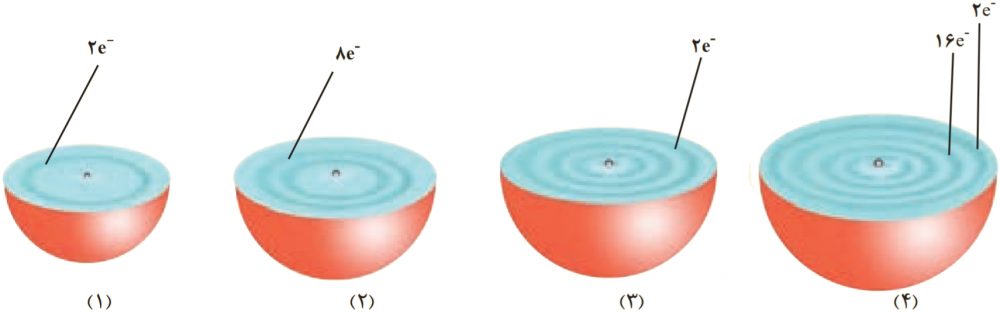
آ) موقعیت هر عنصر را در جدول دورهای تعیین کنید.
| شکل | ۱ | ۲ | ۳ | ۴ |
|---|---|---|---|---|
| نام اتم | ۲He | 10Ne | 12Mg | 28Ni |
| دوره | ۱ | ۲ | ۳ | ۴ |
| گروه | ۱۸ | ۱۸ | ۲ | ۱۰ |
ب) کدام اتم (ها) تمایلی به انجام واکنش و ترکیب شدن ندارد؟ چرا؟
اتم ۲He ، ۱۰Ne ، چون لایه ظرفیت آنها پر است.
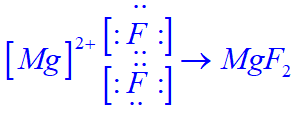
پ) آرایش الکترون نقطهای (۲) و(۳) را رسم و پیشبینی کنید هر یک از این اتمها در واکنش با فلوئور چه رفتاری دارد؟

در اتم نئون همهی الکترونها جفت میباشد و بنابراین تمایلی به واکنش دادن ندارد.
اتم منیزیم ۲ الکترون تکی دارد و تمایل دارد تا به دو اتم فلوئور بدهد و ترکیب منیزیم فلوئورید را بسازد.
ت) در اتم (۴) زیر لایه به طور کامل از الکترونها پر شده است؟ توضیح دهید.
با نوشتن آرایش الکترونی اتم (۴) داریم:
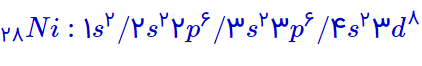
شش زیر لایه به طور کامل از الکترون اشغال شده است.
جواب صفحه ۴۴ شیمی دهم
۱۰) دانش آموزی با استفاده از مدل فضاپرکن کربن دی اکسید مطابق شکل زیر توانست، جرم یک مولکول از آن را برحسب amu به درستی محاسبه کند.

آ) روش کار او را توضیح دهید.
مجموع جرم اتم های سازنده ی آن را بر حسب با هم جمع می کند.
ب) جرم یک مول از مولکول نشان داده شده چند گرم است؟ چرا؟
دلیل تفاوت تقریب در جرم های اتمی و ثابت های به کار رفته (شامل عدد آووگادر و جرم معادل 1amu) می باشد.
پ) جرم مولی کربن دی اکسید را با استفاده از داده ها در جدول دوره ای به دست آورید.

ت) با استفاده از داده های جدول دورهای عنصرها، جرم مولی هریک از ترکیب های زیر را برحسب گرم بر مول به دست آورید.
Cl۲, HCl, NaCl, CaF۲, SO۳, Al۲O۳

۱۱) به پرسش های زیر پاسخ دهید.
آ) پتاسیم سه ایزوتوپ با نمادهای دارد، با توجه به جرم اتمی میانگین پتاسیم در جدول دوره ای عنصرها، مشخص کنید که بیشترین درصد فراوانی مربوط به کدام ایزوتوپ است؟
درصد فراوانی 39𝐾 از دیگر ایزوتوپ ها بیشتر است؛ چرا که وزن جرمی آن به عدد ۳۹ نزدیکتر از دو عدد دیگر است.
ب) جرم دو ایزوتوپ با نمادهای Br(با جرم اتمی ۷۸/۹۲ واحد جرم اتمی) و (با جرم اتمی ۸۰/۹۲ واحد جرم اتمی) دارد و جرم اتمی میانگین آن برابر ۷۹/۹ واحد جرم اتمی است. آیا نتیجه گیری زیر درست است؟ چرا؟
«درصد فراوانی ایزوتوپ های برم تقریبا برابر است.»
بله، درست می باشد؛ زیرا عدد جرمی میانگین آن تقریبا برابر میانگین دو عدد جرمی ایزوتوپ ها می باشد.
۱۲) با مراجعه به جدول دوره ای عنصرها، فرمول چند ترکیب یونی دوتایی را بنویسید که فرمول عمومی آنها به شکل زیر باشد (X و Y می توانند نماینده عنصرهای گوناگون باشند)
(توجه: برای پاسخ دادن به این پرسش، ۱۸ عنصر اول جدول دوره ای عنصرها به جز بریلیم، بور و آلومینیوم را در نظر بگیرید.)
) آ) 𝑁𝑎𝐶𝑙,𝐾𝐶𝑙,𝑀𝑔𝑂,𝐾𝐼,𝐶𝑎𝑂
ب) 𝑁𝑎۲𝑂,𝐾۲𝑂,𝑅𝑏۲𝑆,𝐾۲𝑆,𝑁𝑎۲𝑆
پ) 𝑀𝑔𝐶𝑙۲,𝑀𝑔𝐼۲,𝐶𝑎𝐶𝑙۲,𝐶𝑎𝐼۲,𝑀𝑔𝐹۲
ت) 𝑁𝑎۳𝑁,𝐾۳𝑁,𝑁𝑎۳𝑃,𝐾۳𝑃,𝐾۳𝐴𝑠
جواب صفحه ۴۵ شیمی دهم
۱۳) آ) پژوهشگران در حفاری یک شهر قدیمی، تکه ای از یک ظرف سفالی پیدا کردند. آنها برای یافتن نوع عنصرهای فلزی آن به آزمایشگاه شیمی مراجعه کردند و از این نمونه طیف نشری گرفتند. شکل زیر الگویی از طیف نشری خطی این سفال و چند عنصر فلزی را نشان می دهد. با توجه به آن پیش بینی کنید چه فلزهایی در این سفال وجود دارد؟
مس و کروم
مس و جیوه
کلسیم و کروم

با توجه به طیف نشری خطی متوجه می شویم که مجموع دو طیف مس و جیوه است که در نمونه بوجود آمده است.
ب) طیف های نشری خطی دو نمونه مجهول، طول موج های زیر را نشان می دهند.
(نمونه ۱) ۵۷۸، ۵۲۲، ۵۱۵، ۵۱۱، ۴۸۱، ۴۶۸، ۳۶۱ نانومتر
(نمونه ۲) ۵۲۱، ۴۹۶، ۴۸۵، ۴۶۱، ۴۳۱، ۴۲۹، ۴۲۷، ۴۲۵، ۴۲۱، ۴۰۸، ۳۶۱، ۳۵۷ نانومتر
با توجه به آنها و طیف نشری خطی عنصرهای داده شده در شکل زیر، پیش بینی کنید در هر نمونه چه فلزهایی وجود دارد؟ (گاهی تعدادی از خط های طیف نشری خطی عنصرها به دلیل شدت کم مشاهده نمی شوند.)

جواب صفحه ۴۶ شیمی دهم
۱۴- عنصر Z یکی از عنصرهای دوره سوم جدول دوره ای عنصرهاست که در ساختار آرایش الکترون نقطه ای آن سه الکترون تک (جفت نشده) وجود دارد. اتم این عنصر می تواند در برخی واکنش ها سه الکترون به اشتراک بگذارد و در برخی واکنش ها سه الکترون بگیرد. آرایش الکترونی آن را رسم کنید.
در دوره سوم جدول تناوبی تنها اتم هایی که بتوانند سه الکترون از دست بدهند و یا سه الکترون به دست آورند فقط اتم های Al و P است که بین این دو اتم، فقط اتم P می باشد که می تواند سه الکترون بدهند و سه الکترون به دست آورد. بنابراین آرایش الکترونی آن به صورت زیر است:
۱۵- اتم های زیر را برحسب کاهش تعداد نوترون مرتب کنید.
از تعداد کم (سمت چپ) به تعداد بیشتر نوترون (سمت راست):
۱۶- با مراجعه به جدول دوره ای عنصرها، در کدام گونه های شیمیایی زیر تعداد نوترون ها برابر با مجموع «تعداد پروتون ها و نصف الکترون ها» است؟
فقط در یک گونه چنین خواسته ای از مسئله پیدا می شود:

۱۷- درباره اتم مس (با عدد اتمی ۲۹) در حالت پایه، به پرسش های زیر پاسخ دهید.
آ) آرایش الکترونی آن را نوشته و شماره گروه و دوره آن را تعیین کنید.
ردیف ۴ و گروه ۱۱ جدول تناوبی و آرایش الکترونی آن به صورت زیر است:
ب) چند الکترون با عدد کوانتومی l=0 و چند الکترون با عدد کوانتومی l=2 دارد؟
در زیر لایه s، ۲ الکترون با l=0 ، در زیر لایه p ، ۲ الکترون با l=0 و در زیر لایه d هم ۲ الکترون با l=0 وجود دارد؛ در نتیجه تعداد l=0 برابر ۷ عدد است که وقتی در عدد ۲ ضرب می شود، ۱۴ الکترون می شود، ولی در نهایت ۱ الکترون باید کم کنیم؛ چرا که در بیرونی ترین لایه، یک الکترون وجود دارد.
تنهاترین زیر لایه ای که در این اتم l=2 دارد، فقط d می باشد که ۱ عدد جایگاه l=2 دارد؛ و چون الکترون آن تکمیل است، بنابراین ۲ عدد الکترون با چنان ویژگی خواسته شده در اتم مس می یابیم.
پ) در بیرونی ترین لایه آن چند الکترون وجود دارد؟
در بیرونی ترین لایه آن یعنی n=4 یک الکترون وجود دارد.
ت) در بیرونی ترین زیرلایه آن چند الکترون وجود دارد؟
در بیرونی ترین زیر لایه آن یعنی \(۴{s^1}\) یک الکترون وجود دارد.
ث) چند زیرلایه نیمه پر و پر وجود دارد؟
۶ زیر لایه پر و یک عدد زیر لایه نیمه پر داریم.
برای مشاهده گام به گام سایر صفحات کتاب کافیست آن را در گوگل به همراه عبارت «حالا درس» جست و جو کنید.

۲۵ دیدگاه ها
مرسی❤
مرسی خوب بود????❤
سوال ۱۷ ب اشتباه حل شده!!
در واقع باید زیر لایه s ۷ الکترون و d ۱۰ الکترون داشته باشه
خدا خیرت بده
ناقص ناقص بود اصلا خوب نبود افتضاح
خییییلی خییییییییییییییلی خییییییییییییییلی افتضاااح
سوال های ۱۲ و ۱۴ ۱۵ کامل نیست
بعضی هارو جواب ندادین
بسیار مفید بود
پس جواب سوال ۶ و ۱۲؟
بازم ممنون
یا انجام ندید،یا میخواید انجام بدید کامل انجام بدید.از اینکه چنتارو انجام ندادین متشکرم????
بعضی ها اشتباه بود
تنکیووووووووو
عالی
عالیییییییییییییییییییییییییییییی♥????
بسیار عالی ????
فقط پاسخ سوال ۱۲ نبود
خیلی از جواب های تان اشتباه بود
عالی و کامل
جواب سوال ۱۴ و ۱۵ کامل نیست
۱۵جواب ندادی
۱۴ جواب ندادی
۱۶ جواب ندادی
عالی
عالی