جواب با هم بیندیشیم صفحه ۱۱۱ شیمی دهم
در این نوشته با جواب با هم بیندیشیم صفحه ۱۱۱ شیمی دهم همراه شما هستیم.
جواب با هم بیندیشیم صفحه ۱۱۱ شیمی دهم
۱) با توجه به مقدار گشتاور دو قطبی هر ماده، موارد زیر را توجیه کنید.
آ) انحلال استون در آب
آب و استون – هر دو از مولکول های قطبی تشکیل شده اند از این رو استون در آب حل می شود.
ب) انحلال یُد در هگزان
ید و هگزان مولکول هایی غیر قطبی هستند، به همین دلیل با یکدیگر حل شده و یک محلول همگن بوجود می آید.
پ) حل نشدن هگزان در آب
چون هگزان ناقطبی ست نمی تواند بر پیوند های قطبی مولکول های آب غلبه کند از این رو هگزان در آب حل نمی شود و یک مخلوط ناهمگن پدید می آید.
۲) آیا جمله «شبیه شبیه را حل می کند» درست است؟ توضیح دهید.
بلی – تجربه و آزمایش نشان می دهد که حل شونده های قطبی در حلال های قطبی و حل شونده های ناقطبی در حلال های ناقطبی بهتر حل می شوند.
۳) آزمایش ها نشان می دهد که فرایند انحلال هنگامی منجر به تشکیل محلول می شود که:
( میانگین جاذبه ها در حلال خالص وحل شونده خالص ) بزرگتر است از ( جاذبه های حل شونده با حالل در محلول )
با این توصیف با توجه به شکل زیر، به پرسش های مطرح شده پاسخ دهید.
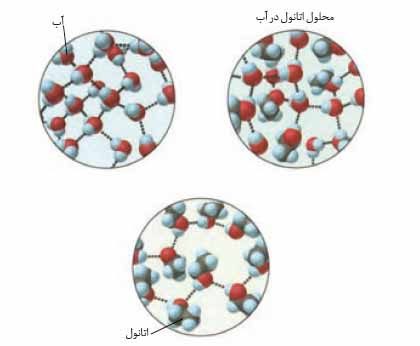
آ) نیروهای بین مولکولی در هریک از چه نوعی است؟ چرا؟
چون هم در مولکول آب و هم در مولکول اتانول پیوند هیدروژنی وجود دارد درمحلول این دو نیز میان ملکول های آب و اتانول پیوند هیدروژنی برقرار می شود.
ب) عبارت زیر را با علامت کوچکتر یا بزرگتر کامل کنید.
لازمه انحلال اتانول در آب , شکسته شدن پیوند هیدروژنی میان مولکول های اتانول – اتانول و آب – آب است و چون اتانول در آب حل می شود می توان نتیجه گرفت که در مجموع انرژی حاصل از تشکیل پیوند هیدروژنی جدید میان مولکول های آب و اتانول توانسته است پیوند های هیدروژنی اولیه را بشکند. یعنی میانگین انرژی پیوند آب – اتانول از میانگین انرژی پیوند آب – آب و اتانول – اتانول بیشتر است و چون دمای جوش آب از اتانول بیشتر است می توان گفت انرژی پیوند هیدروژنی در مولکول های آب از انرژی پیوند هیدروژنی در مولکول های اتانول بیشتر است.
پ) چرا شیمی دان ها انحلال اتانول در آب را انحلال مولکولی می نامند؟ توضیح دهید.
با انحلال اتانول در آب , ساختار مولکولی اتانول دچار تغییر نمی شود بلکه مولکول های اتانول میان مولکول های آب پراکنده می شود.
برای مشاهده گام به گام سایر صفحات کتاب کافیست آن را در گوگل به همراه عبارت «حالا درس» جست و جو کنید.
