جواب خود را بیازمایید صفحه ۳۳ و ۳۴ شیمی دهم

در این نوشته با جواب خود را بیازمایید صفحه ۳۳ و ۳۴ شیمی دهم همراه شما هستیم.
جواب صفحه ۳۳ و ۳۴ شیمی دهم
۱- آ) با مراجعه به جدول دوره ای عنصرها، جدول زیر را کامل کنید.
| نماد عنصر | ۳Li | ۸O | ۱۰Ne | ۱۴Si | ۲۰Ca | ۲۷Co | ۳۵Br |
|---|---|---|---|---|---|---|---|
| شمارۀ گروه | ۱ | ۱۶ | ۱۸ | ۱۴ | ۲ | ۹ | ۱۷ |
| شمارۀ دوره | ۲ | ۲ | ۲ | ۳ | ۴ | ۴ | ۴ |
ب) جدول زیر را کامل کنید.
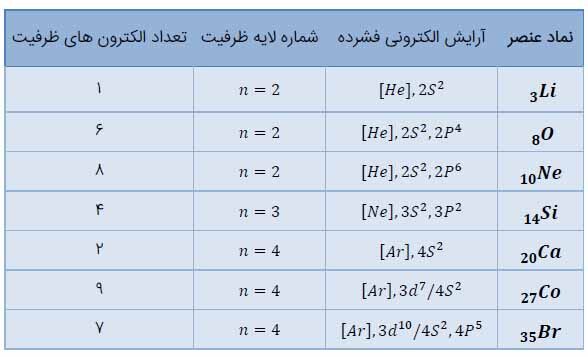
پ) از روی آرایش الکترونی اتم هر عنصر میتوان موقعیت آن را در جدول تعیین کرد، برای این منظور:
* شمارۀ بیرونیترین لایه را با شمارۀ دوره این عنصرها مقایسه کنید. از این مقایسه چه نتیجهای میگیرید؟
شماره دوره همان شماره لایه ظرفیت است. عناصری که آرایش الکترونی آنها به ( ۳d ) ختم میشود در دورهی چهارم جای دارند.
* شمارۀ گروه کدام عنصرها با تعداد الکترونهای ظرفیت آنها برابر است؟
۳𝐿𝑖 ، 20𝐶𝑢 ، 27𝐶𝑜
* شمارۀ گروه کدام عنصرها با تعداد الکترونهای ظرفیت آنها برابر نیست؟ در این حالت بین شمارۀ گروه و تعداد الکترونهای ظرفیت چه رابطهای هست؟ توضیح دهید.
عناصری که زیر لایه (s و d) آنها در حال پر شدن است شمارهی گروه با تعداد الکترونهای ظرفیتی آنها برابر است
عناصری که زیر لایه (p) آنها در حال پر شدن میباشد با اضافه کردن عدد ۱۰ بر تعداد الکترونهای ظرفیتی میتوان به شمارهی گروه این عناصر پی برد.
* برای عنصرهای دستۀ d، شمارۀ دوره و گروه را چگونه میتوان از روی آرایش الکترونی به دست آورد؟ توضیح دهید.
عناصر دستهی (d) دارای شمارهی دوره ( n+1 ) هستند. برای مثال اگر آرایش الکترونی زیر لایه به ۳d۷ ختم شود
دوره آن عبارت است از (۴=۱+۳) و برای به دست آوردن شماره گروه میتوان تعداد الکترون ظرفیت را منظور کرد (به جز عناصر کروم و مس که دارای آرایش الکترونی استثناء بوده و به ترتیب در گروههای ۶ و ۱۱ جدول تناوبی جای دارند.
۲) موقعیت عنصرهای کربن (C (با عدد اتمی ۶))، کربن (Al (با عدد اتمی ۱۳))، کربن (Fe (با عدد اتمی ۲۶)) و کربن (Zn (با عدد اتمی ۳۰)) را در جدول دوره ای عنصرها تعیین کنید.
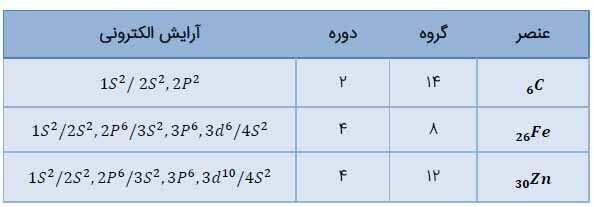
۳- عنصرهای جدول دورهای را میتوان در چهار دسته به صورت زیر جای داد:
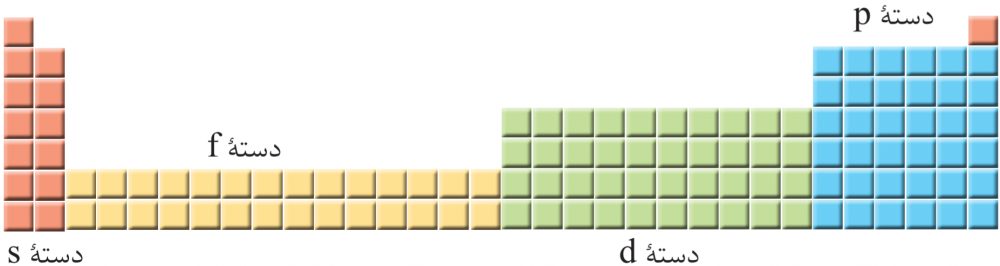
اساس این دسته بندی را توضیح دهید.
عناصر جدول تناوبی در چهار دستهی s, p , d , f قرار میگیرند. طبق اصل آفبا، بر اساس آرایش الکترونی لایه ظرفیت و بیرونیترین زیرلایه، اتمها را در دوره و گروههای مشخص طبقه بندی میکنند. عناصری که در هر گروه از جدول قرار دارند دارای آرایش الکترونی لایه ظرفیت مشابهی هستند.
برای مشاهده گام به گام سایر صفحات کتاب کافیست آن را در گوگل به همراه عبارت «حالا درس» جست و جو کنید.
